2 英文参考
胰凝乳朊酶
chymotrypsin
alfapsin
alphachymar
alpha-chymarophth
alpha-chymotrypsin
avazyme
catarase
chymar
chymolase
5 糜蛋白酶药典标准
5.1 品名
5.1.1 中文名
5.1.2 汉语拼音
Midanbaimei
5.1.3 英文名
Chymotrypsin
5.2 来源含量
本品系自牛或猪胰中提取的一种蛋白分解酶。按干燥品计算,每1mg糜蛋白酶的活力不得少于1000单位。
5.3 制法要求
本品应从检疫合格的牛或猪胰中提取,生产过程应符合现行版《药品生产质量管理规范》要求。
5.4 性状
本品为白色或类白色结晶性粉末或无定型粉末。
5.5 鉴别
取本品,加水溶解并制成每1ml中约含1mg的溶液,取0.05ml置白色点滴板上,加N-乙酰-L-酪氨酸乙酯试液0.2ml,混匀后,显紫红色。
5.6 检查
5.6.1 酸度
取本品,加水溶解并制成每1ml中含2mg的溶液,依法测定(2010年版药典二部附录Ⅵ H),pH值应为5.5~7.0。
5.6.2 溶液的澄清度与颜色
取本品,加水溶解并制成每1ml中含2mg的溶液,依法检查(2010年版药典二部附录Ⅸ A和2010年版药典二部附录Ⅸ B),溶液应澄清无色或几乎无色。
5.6.3 胰蛋白酶
取本品,加水溶解并制成每1ml中含16000单位的溶液,作为供试品溶液;取胰蛋白酶适量,加水溶解并制成每1ml中含2500单位的溶液,作为对照溶液。取供试品溶液50μl与对照溶液5μl,分别置白色点滴板上,各加对甲苯磺酰-L-精氨酸甲酯盐酸盐试液0.2ml,放置后,供试品溶液应不呈现紫红色或呈色时间迟于胰蛋白酶对照溶液。
5.6.4 干燥失重
取本品约0.2g,以五氧化二磷为干燥剂,在60℃减压干燥4小时,减失重量不得过5.0%(2010年版药典二部附录Ⅷ L)。
5.6.5 炽灼残渣
不得过2.5%(2010年版药典二部附录Ⅷ N)。
5.7 效价测定
5.7.1 底物溶液的制备
取N-乙酰-L-酪氨酸乙酯23.7mg,置100ml量瓶中,加磷酸盐缓冲液(取0.067mol/L磷酸二氢钾溶液38. 9ml与0.067mol/L磷酸氢二钠溶液61.1ml,混合,pH值为7.0)50ml,温热使溶解,冷却后再稀释至刻度,摇匀。冰冻保存,但不得反复冻融。
5.7.2 供试品溶液的制备
精密称取本品适量,加0.0012mol/L盐酸溶液溶解并定量稀释制成每1ml中含12~16糜蛋白酶单位的溶液。
5.7.3 测定法
取0.0012mol/L盐酸溶液0.2ml与底物溶液3.0ml,照紫外-可见分光光度法(2010年版药典二部附录Ⅳ A),在25℃±0.5℃,于237nm的波长处测定并调节吸光度为0.200。再取供试品溶液0.2ml与底物溶液3.0ml,立即计时并摇匀,每隔30秒钟读取吸光度,共5分钟(重复一次),吸光度的变化率应恒定,恒定时间不得少于3分钟。若变化率不能保持恒定,可用较低浓度另行测定。每30秒钟的吸光度变化率应控制在0.008~0.012,以吸光度为纵坐标,时间为横坐标,作图,取在3分钟内成直线部分的吸光度,按下式计算。

A2为直线上开始的吸光度;
A1为直线上终止的吸光度;
T为A2至A1读数的时间,分钟;
W为测定液中含供试品的量,mg;
0.0075为在上述条件下,吸光度每分钟改变0.0075,即相当于1个糜蛋白酶单位。
5.8 类别
蛋白分解酶。
5.9 贮藏
5.10 制剂
5.11 版本
《中华人民共和国药典》2010年版
6 糜蛋白酶的医学检查
6.1 检查名称
6.2 分类
6.3 糜蛋白酶的测定原理
同RIA测定法原理。
6.4 试剂
(1)血清、血浆(EDTA抗凝)标本均可,保存条件同胰蛋白酶。
(2)大便,0.15mol/L NaCl+倍稀释,搅匀,然后过滤,滤液室温条件下可保存1周。
6.5 操作方法
RIA法。
6.6 正常值
血清 10μg/L
6.7 化验结果临床意义
6.8 附注
(1)口服酶制剂可致升高。
(2)这是检测与胰腺分泌功能不全相联系的胰腺疾病的筛选实验,进一步排查那些胰腺功能貌似正常的患者,大便中胰凝乳蛋白酶(chymotrypsin)测定是一个较胰蛋白酶活性更可靠的胰腺功能评估方法。
(3)假阳性结果也很多,均为10%左右,有时在上述疾病患者中也会出现正常值。
6.9 相关疾病
7 糜蛋白酶介绍
7.1 药品名称
7.2 英文名称
Chymotrypsin
7.3 别名
7.4 分类
7.5 剂型
注射用糜蛋白酶每支1mg(800U);5mg(4000U)。
7.6 糜蛋白酶的药理作用
可将蛋白质大分子的肽链切断,成为分子量较小的肽,或在蛋白分子肽链端上作用,使氨基酸分出;并可将某些脂类水解。通过此作用能使痰中纤维蛋白和粘蛋白等水解为多肽或氨基酸,使粘稠痰液液化,便于咳出,对脓性或非脓性痰都有效。此外,糜蛋白酶尚能松弛睫状韧带及溶解眼内某些组织的蛋白结构。糜蛋白酶还有促进抗生索、化疗药物向病灶渗透的作用。
7.7 糜蛋白酶的药代动力学
糜蛋白酶和胰蛋白酶都是强力蛋白水解酶,仅水解部位有差异。蛇毒神经毒含碱性氨基酸,易被糜蛋白酶和胰蛋白酶分解为无毒蛋白质,从而阻断毒素进入血流产生中毒作用。糜蛋白酶对蝮亚科蛇伤疗效优于胰蛋白酶,两种酶制剂联合应用效果更佳。
7.8 糜蛋白酶的适应证
1.用于眼科于术松弛睫状韧带、减轻创伤性虹膜睫状体炎;也可用于白内障摘除,使晶体易于移去。
2.用于创伤或手术后伤口愈合、抗炎及防止局部水肿、积血、扭伤血肿、乳房手术后浮肿、中耳炎、鼻炎等。
3.用于慢性支气管炎、支气管扩张或肺脓肿的治疗,可使脓性和非脓性痰液均可液化,易于咳出。
4.毒蛇咬伤的处理。
7.9 糜蛋白酶的禁忌证
1.20岁以下的患者,由于晶体囊膜玻璃体韧带相连牢固,眼球较小,巩膜弹性强可致玻璃体脱出,或玻璃体液不固定的创伤性白内障病人,因可导致玻璃体液丧失,故均禁用。
2.眼压高或伴有角膜变性的白内障患者,以及玻璃体有液化倾向者均禁用。
7.10 注意事项
3.糜蛋白酶对视网膜有较强的毒性,由于可造成晶体损坏,应用时勿使药液透入玻璃体。
4.糜蛋白酶遇血液迅速失活,因此在用药部位不得有末凝固血液。
5.糜蛋白酶在固体状态时比较稳定,但其溶液不稳定,室温放置9天可损失50%的活性,故应临用前配制。
6.对糜蛋白酶引起的青光眼症状,于术后滴用β-受体阻滞药(如噻吗洛尔)或口服碳酸酐酶抑制药(如乙酰唑胺),可能会缓解。
7.由于超声雾化后糜蛋白酶效价下降明显,因此,糜蛋白酶超声雾化吸入时间宜控制在5min内。
7.11 糜蛋白酶的不良反应
1.眼科局部用药一般不会引起全身不良反应,但可引起短期眼压增高,导致眼痛、眼色素膜炎和角膜水肿,这种青光眼症状可持续1周后消退,还可导致角膜线状混浊、玻璃体疝、虹膜色素脱落、葡萄膜炎及创口开裂或延迟愈合等。
3.其他:(1)肌内注射偶可致过敏性休克。(2)糜蛋白酶可引起组胺释放,导致局部注射部位疼痛、肿胀。
7.12 糜蛋白酶的用法用量
1.通常一次4000U,用前将糜蛋白酶以氯化钠注射液5ml溶解。
2.经眼给药:用于眼科作为酶性分解晶状体悬韧带,以氯化钠注射液溶解糜蛋白酶,配成1∶5000溶液,从瞳孔注入后房,经2~3min,在晶体浮动后,用氯化钠注射液冲洗,即可取出晶状体。
4.局部注射:(1)在处理软组织炎症或创伤时,可用糜蛋白酶800U(1mg)溶于1ml的生理氯化钠溶液的药液局部注于创面。(2)毒蛇咬伤,糜蛋白酶10~20mg,每支用注射用水4ml稀释后,以蛇牙痕为中心向周围作浸润注射,并在伤口中心区域注射2针,再在肿胀上方3cm处作环状封闭1~2层,根据不同部位每针0.3~0.7ml,至少10针,最多26针。
5.外用:(1)寻常痤疮,糜蛋白酶局部涂搽,每天2次。(2)慢性皮肤溃疡,糜蛋白酶(400μg/ml)水溶液,湿敷创面,每次1~2h。
7.13 药物相互作用
(尚不明确)
7.14 专家点评
糜蛋白酶用途广泛,尚可用于扭伤、中耳炎、鼻炎、鼻窦炎、咽炎、肺脓疡等治疗。可用于外科炎症、创伤、血肿及脓肿等,也可用于气管切开术。糜蛋白酶对痰多患者效果较好,使痰易于咳出。
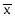 :290)
:290)