1 拼音
chāo shēng duō pǔ lè tāi ér jiān hù yí chǎn pǐn zhù cè jì shù shěn chá zhǐ dǎo yuán zé
《超声多普勒胎儿监护仪产品注册技术审查指导原则》由国家食品药品监督管理局于2012年5月10日食药监办械函[2012]210号印发。
本指导原则旨在指导和规范超声多普勒胎儿监护仪产品的技术审评工作,帮助审评人员增进对该类产品原理、结构、主要性能、预期用途等方面的理解,把握技术审评工作的基本要求和尺度,以便对产品安全性、有效性作出系统评价。
本指导原则是对超声多普勒胎儿监护仪的一般要求,申请人/生产企业应依据具体产品的特性对注册申报材料的内容进行充实细化。
本指导原则是对产品的技术审查人员和申请人/生产企业的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行。
本指导原则是在当前认知水平下制订的,随着科学技术的不断发展,本指导原则的相关内容也将进行适时的调整和更新。审查人员仍需密切关注相关适用的标准以及注册法规的变化,以确认申报的产品是否符合法规的要求。
2 一、 适用范围
本指导原则适用于《医疗器械分类目录》中6823-3中“超声母婴监护设备”中的超声多普勒胎儿监护仪。如果超声多普勒胎儿监护仪作为一个系统中的一部分,则本指导原则也适用于该部分。
本指导原则不适用于超声多普勒胎儿心率仪,超声多普勒胎儿心率仪指根据多普勒原理从孕妇腹部获取胎儿心脏运动信息,不用作连续监护,仅获取胎儿心脏运动信息。该类仪器采用的行业标准为YY O448-2009《超声多普勒胎儿心率仪》。
本指导原则所涉及的超声多普勒胎儿监护仪,其定义采用YY O449-2009《超声多普勒胎儿监护仪》3.1,即“由主机、超声探头、宫缩压力传感器及与之相连接的仪器组成,采用超声多普勒原理,具有监测和贮存胎心率、宫缩数据的功能,并可设置报警。”
3 二、 技术审查要点
3.1 (一) 产品名称的要求
产品名称应以发布的国家标准、行业标准以及《医疗器械产品分类目录》中的产品名称为依据。产品名称应以体现产品的工作原理、技术结构特征、功能属性为基本准则。如“超声胎儿监护仪”,“超声母亲/胎儿综合监护仪”等,不宜采用病症命名。
3.2 (二) 产品的结构和组成
一般由主机、超声探头、宫缩压力传感器及与之相连接的仪器组成。一般的结构示意框图如下:
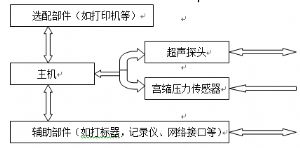
对超声多普勒胎儿监护仪及其部件进行全面评价所需的基本信息应包含但不限于以下内容:
1.产品设计和说明
应包括对产品工作原理的概述,该部分内容应当包括:
1.1 产品构成说明
1.1.1 整机总体构造的详细描述,应包括所有组成部分,应给出有标记的图示(如图表、照片和图纸等),清楚的标识关键部件/组件,其中包括充分的解释来方便理解这些图示。
1.1.2对使用者可接触的所有控制装置的说明,包括但不限于:
1.1.2.1控制设置范围;
1.1.2.2缺省值(如果有)。
1.1.3 产品工作框图(应包括所有应用部分,以及信号输入和输出部分)。
1.1.4 对所有组件的全面描述,至少包括:
1.1.4.1传感器的规格、参数、工作方式、超声换能器的输出功率和声强等;
1.1.4.2所有附件、配件的列表;
1.1.4.3拟配合使用的设备或部件,并应对接口进行描述。
1.2 接触患者(孕妇)的材料
应有直接接触或间接接触患者(孕妇)的材料的组成清单,应提供所有材料的商品名称和基本成分名称(如聚乙烯、聚碳酸酯等)。应根据GB/T 16886等标准给出所用材料的生物相容性评价。
3.3 (三) 产品工作原理
超声多普勒胎儿监护仪采用超声多普勒原理对孕妇及胎儿进行连续监护,并在出现异常时及时提供报警信息。一般系附在孕妇腹部,通常采用多元扁平超声多普勒换能器。
超声多普勒胎儿监护仪可实时监护胎儿心跳等变化情况,为临床提供准确的诊断及处理资料,它既可单独使用,也可通过网络接口与产科中央监护系统连接,形成一套有中央站的网络监护系统,也可以同时提供多种移动应用解决方案。
检测胎儿心率信号经处理后将胎儿心率变化趋势用轨迹描记出来,并能同时插记母体的宫缩曲线。
医生根据这二条曲线的变化趋势可以初步判断胎儿的健康情况,以便及时采取措施、保障胎儿健康,提高新生儿质量。
超声多普勒胎儿监护仪所使用的超声波生物物理特性主要有机械效应、热效应和空化效应。具体产品可能涉及以上全部或部分效应。但其强度一般很低。
3.4 (四) 产品作用机理
超声多普勒胎儿监护仪作为非治疗设备,其设备向人体传送能量和从人体取得能量以获取所需信息。该产品用于诊断、监护,不以治疗为目的,所以超声声输出的强度应尽可能的低。
3.5 (五) 产品适用的相关标准
下列文件对于本指导原则的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 191-2008《包装储运图示标志》
GB 9706.1-2007《医用电气设备 第1部分:安全通用要求》(IEC 60601-1:1988,IDT)
GB 9706.9—2O08《医用电气设备 第2-37部分:医用超声诊断和监护设备安全专用要求》(IEC 60601-2-37:2004,IDT)
GB 9706.15-2008《医用电气设备 第1-1部分:安全通用要求 并列标准:医用电气系统安全要求》(IEC 60601-1-1:2000,IDT)
GB/T 14710-2009《医用电器环境要求及试验方法》
GB/T 16886.1-2011《医疗器械生物学评价 第1部分:评价与试验》
YY 0505-2005《医用电气设备 第1-2部分:安全通用要求 并列标准:电磁兼容要求和试验》
YY0709-2009《医用电气设备 第1-8部分:并列标准 安全通用要求 医用电气设备和医用电气系统中报警系统的测试和指南》
YY/T 1142—2003《超声诊断和监护仪器频率特性的测试方法》
3.6 (六) 产品的预期用途
主要用于监测胎儿的心率和胎动以及宫缩压力,对孕妇及胎儿进行连续监护,并在出现异常时及时提供报警信息。
3.7 (七) 产品的主要风险
1.超声多普勒胎儿监护仪的风险管理报告应符合YY/T 0316-2008《医疗器械 风险管理对医疗器械的应用》中的相关要求,判断与产品有关的危害估计和评价相关的风险,控制这些风险并监视风险控制的有效性。申请人提供注册产品的风险管理报告应扼要说明:
(1)在产品的研制阶段,已对其有关可能的危害及产生的风险进行了估计和评价,并有针对性地实施了降低风险的技术和管理方面的措施;
(2)在产品性能测试中部分验证了这些措施的有效性,达到了通用和相应专用标准的要求;
(3)对所有剩余风险进行了评价;
(4)全部达到可接受的水平;
2.风险管理报告的内容至少包括:
(3)产品应符合的安全标准;
申报方应按照YY/T0316-2008《医疗器械 风险管理对医疗器械的应用》附录C的34条提示,对照产品的实际情况作出针对性的简明描述。
注意:产品如存在34条提示以外的可能影响安全性的特征,也应作出说明。
申报方应根据自身产品特点,根据YY/T 0316-2008附录E的提示,对危害、可预见事件序列、危害处境及可导致的损害作出判定。表1所列为超声多普勒胎儿监护仪的常见危害:
编号 | 可预见的事件序列 | 危害处境 | 损害 | |
1 | ||||
1.1 | 电能 | |||
1.1.1 | 电源输入插头剩余电压 | 导致对孕妇电击伤害 | ||
1.1.2 | 过量的漏电流 | 绝缘/隔离效果不符合要求 | ||
1.1.3 | 通过应用部分(探头、宫缩传感器)引起孕妇触电 | 1. 隔离措施不足; 2. 电介质强度达不到要求; | ||
1.1.4 | 误接触高压部分 | 1. 安全地线没有或失效; 2. 高压绝缘介质年久老化,绝缘性能下降,导致高压击穿 | ||
1.2 | 热能 | |||
1.2.1 | 非预期的或过量的传感器表面温升 | 传感器压电晶片振动的机械耗损、声阻抗匹配不佳引起的损耗和高压开关损耗 | ||
1.2.2 | ||||
1.3 | ||||
1.3.1 | ||||
1.3.2 | ||||
1.4 | 机械力 | |||
1.4.1 | 操作者缺乏相关常识 | 孕妇腹部压力过大,引起被孕妇不适 | ||
1.4.2 | 锐边或尖角 | 主机或/和治疗头表面有锐边或尖角 | 使用者和孕妇被划伤 | |
2 | ||||
2.1 | 生物不相容性 | 1. 与孕妇接触的传感器材料有致敏性; 2. 与孕妇接触的传感器材料有刺激性; | ||
3 | ||||
3.1 | 设备受到外界的电磁干扰 | 1. 产品设计时电磁屏蔽及电路抗扰设计不充分; | 不能正常工作 | |
3.2 | 1. 屏蔽、滤波及接地技术不完善; | 引起其他设备不能正常工作 | ||
4 | 器械使用的危害 | |||
4.1 | 误操作 | 1. 未经培训的人员使用操作 | 使被孕妇不适 | |
4.2 | 使孕妇皮肤造成不适 | |||
4.3 | 交叉感染 | 可导致感染性疾病 | ||
4.4 | 工作数据的准确性 | 监测数据不准确 | 导致正确状态误报或危险状态不报 | |
(6)明确风险可接受准则。
(7)对所判定的危害确定初始风险控制方案,列出控制措施实施证据清单。
3.8 (八) 产品的主要技术指标
1.安全要求:
至少包括以下要求:
1.1 电气安全应当符合GB 9706.1,GB 9706.9、GB9706.15和YY 0505的要求。
1.2 生物相容性,直接接触或间接接触患者(孕妇)或操作者的材料组成,应当进行生物相容性评价(参见《医疗器械生物学评价和审查指南》),并给出清单,提供所有材料的商品名称和基本成分名称(如铝合金、硅橡胶、聚乙烯、聚碳酸酯等)。
至少包括以下要求:
2.1超声输出
胎心率的测量和显示范围不窄于65次/min~210次/min。
2.2 报警功能
仪器应装有发光或发声的报警装置,在测量胎心率超过预置值时,应产生报警信号,并可消除警报。从胎心率越限至开始报警的时间不大于30s。
2.3 宫缩压力测量范围
宫缩压力的测量范围应覆盖0~100单位,其非线性误差不大于±10%。
2.4 贮存记录功能
2.4.1 内置实时记录器的仪器其走纸速度的误差不超过±5%。
2.4.2 内置实时记录器的基线漂移不大于全量程的5%。
2.5 功能要求
3.环境试验要求
生产企业应在产品标准中按GB/T14710规定气候环境试验和机械环境试验的组别,试验要求及检测项目,按YY 0449-2009表1执行。
3.9 (九)产品的检测要求
性能要求一般至少应包括标准YY0449-2009《超声多普勒胎儿监护仪》中的5.2胎心率测量和显示范围、 5.4报警功能、 5.5宫缩压力测量范围和5.10功能要求;
安全要求至少应包括:漏电流、保护接地阻抗(如适用),电介质强度可考虑抽样检验。
3.10 (十) 产品的临床要求
1.符合《医疗器械注册管理办法》附件12规定,执行国家标准、行业标准的超声多普勒胎儿监护仪,国内市场上已有同类型产品,可以不提供临床试验资料。
2.生产企业在申报超声多普勒胎儿监护仪产品注册时,可以提交已上市同类产品的临床试验资料,同时提交申报产品与已上市同类产品的对比说明。对比说明的内容应当包括:产品结构组成、工作原理、主要技术性能指标、关键部件、预期用途等内容。
(4)宫缩压力测量范围
(5)贮存记录功能
3.不符合上述条件的,生产企业在申报超声多普勒胎儿监护仪产品注册时,应提交完整的临床试验资料。临床试验机构应为国家食品药品监督管理局认定公布的药品临床试验基地。临床试验应按照《医疗器械临床试验规定》以及《医疗器械注册管理办法》附件12的要求进行。
3.11 (十一)产品的不良事件历史记录
暂未见相关报道。
3.12 (十二)产品介绍、标签、包装标识
产品使用说明书应当符合《医疗器械介绍、标签和包装标识管理规定》(国家食品药品监督管理局令第10号)的要求以及GB 9706.1-2007、GB 9706.9—2O08和/或GB 9706.15-2008的相关要求。
由于超声多普勒胎儿监护仪是通过一定量的超声能量作用于人体达到医学监测的目的,在以上的规定和标准中,涉及慎重使用的部分应尽可能详细,清楚,以提示使用者慎重使用。
1.安全预防措施;
2.图标符号的说明,特别是危险符号,注意事项符号的说明;
3.电磁兼容性的说明,提示用户,电磁信号有可能对本产品产生干扰;
4.声输出资料的公布说明;
5.产品的安装,连接。
产品的标签,外部标记中特别是涉及安全使用的部分也应符合相关的标准(如GB9706系列标准等)。
3.13 (十三)注册单元划分的原则
超声多普勒胎儿监护仪的注册单元划分应以《医疗器械注册管理办法》为依据,一般以基本工作原理、主要技术结构、性能指标、预期用途为划分条件。
1.不同的工作原理、技术结构产品应作为不同的注册单元进行注册。
2.主要性能指标差异较大的、或不能覆盖两种或两种以上的超声多普勒胎儿监护仪应考虑划分为不同的注册单元。
3.14 (十四)同一注册单元中典型产品的确定原则和实例
同一注册单元应按产品风险与技术指标的覆盖性确定典型产品。一般来说,典型产品应是同一注册单元内能够代表本单元内其他产品安全性和有效性的产品,即功能最全、结构最复杂和风险最高的产品。在同一注册单元中,若仅辅助功能不同,则可以作为同一产品的多个型号加以区分。
如某企业生产的具有不同辅助功能的超声多普勒胎儿监护仪,其主要性能指标一致[见本指导原则(八)2.1—2.5],可作为同一注册单元,在同一注册单元的两个型号中,A型号具有一种辅助功能,B型号具有两种以上辅助功能并包括前者,或A型号的性能和功能是B型号的子集,应选取B型号作为典型产品。
4 三、 审查关注点
(一)产品的性能要求和安全要求是否执行了规定国家和行业的强制性标准。
1.技术指标[见本指导原则(八)2.1—2.5)];
2.预期用途;
3.关键零部件(探头或传感器)。
(五)介绍必须告知用户的信息是否完整以及外部标记是否符合相关的要求。
(六)注册单元的划分。
(七)关注声输出资料的公布。
5 编写说明
5.1 一、指导原则编写的目的
本指导原则用于指导和规范超声多普勒胎儿监护仪在注册申报过程中审评人员对注册材料的技术审评。
超声多普勒胎儿监护仪是借助超声能量作用对患者(孕妇)予以监测,其临床适用较为广泛。本指导原则旨在让初次接触该类产品的注册审评人员对产品的原理、结构、主要性能、预期用途等各个方面有一个基本的了解,同时让技术审评人员在产品注册技术审评时把握基本的尺度,以确保产品的安全、有效。
5.2 二、指导原则编写的依据
(一)《医疗器械监督管理条例》
(二)《医疗器械注册管理办法》(16号令)
(三)《医疗器械临床试验规定》(5号令)
(四)《医疗器械介绍、标签和包装标识管理规定》(10号令)
(五)《医疗器械标准管理办法》(31号令)
(六)关于印发《境内第一类医疗器械注册审批操作规范(试行)》和《境内第二类医疗器械注册审批操作规范(试行)》的通知(国食药监械[2005]73号)
(七)国家食品药品监督管理局发布的其他规范性文件
(八)相关标准
GB/T 191-2008《包装储运图示标志》
GB 9706.1-2007《医用电气设备 第1部分:安全通用要求》(IEC 60601-1:1988,IDT)
GB 9706.9—2O08《医用电气设备 第2-37部分:医用超声诊断和监护设备安全专用要求》(IEC 60601-2-37:2004,IDT)
GB 9706.15-2008《医用电气设备 第1-1部分:安全通用要求 并列标准:医用电气系统安全要求》(IEC 60601-1-1:2000,IDT)
GB/T 14710-2009《医用电器环境要求及试验方法》
GB/T 16886.1-2001《医疗器械生物学评价 第1部分:评价与试验》
YY 0505-2005《医用电气设备 第1-2部分:安全通用要求 并列标准:电磁兼容要求和试验》
YY 0709-2009《医用电气设备 第1-8部分:并列标准 安全通用要求 医用电气设备和医用电气系统中报警系统的测试和指南》
YY/T 1142—2003《超声诊断和监护仪器频率特性的测试方法》
5.3 三、指导原则中部分具体内容编写的考虑
(一)性能指标以超声多普勒胎儿监护仪的产品标准YY 0449-2009 《超声多普勒胎儿监护仪》为依据。产品的主要技术指标及工作原理的制定征求了全国医用电器标准化技术委员会超声设备分技术委员会的意见,并在一定范围内召开了专家咨询会和多次集体讨论,本内容主要依据现行有效的行业标准YY 0449-2009超声多普勒胎儿监护仪,今后如有修订,应按照新标准的要求执行。
(二)安全要求以GB 9706.1-2007《医用电气设备 第1部分:安全通用要求》(IEC 60601-1:1988,IDT)为依据。
(三)风险管理的要求主要以YY/T0316-2008《医疗器械 风险管理对医疗器械的应用》为依据。
(四)“产品介绍、标签、包装标识”部分以国家相关的法规和相关标准为依据,没有具体地在指导原则中阐述,仅对“慎重使用”部分作了提示。
5.4 四、指导原则的编写人员
本指导原则的编写人员由湖北省食品药品监督管理局医疗器械行政审批人员、技术审批人员、国家食品药品监督管理局湖北医疗器械质量监督检验中心的有关专家共同组成。在编写过程中,征求了有关检测机构、临床医疗机构及国内部分生产企业的意见,以充分利用各方面的信息和资源,尽量确保指导原则的正确、全面、实用。