1 拼音
W S / T 4 7 8 — 2 0 1 5 xuè qīng 2 5 - qiǎng jī wéi shēng sù D 3 jiǎn cè cāo zuò zhǐ nán tóng wèi sù xī shì yè xiāng sè pǔ chuàn lián zhì pǔ fǎ
2 英文参考
Operating guidelines for measurement of serum 25-hydroxyvitamin D3-Isotope dilution liquid chromatography tandem mass spectrometry
3 基本信息
ICS 11.020
C 50
中华人民共和国卫生行业标准WS/T 478—2015《血清25-羟基维生素D3检测操作指南 同位素稀释液相色谱串联质谱法》(Operating guidelines for measurement of serum 25-hydroxyvitamin D3-Isotope dilution liquid chromatography tandem mass spectrometry)由中华人民共和国国家卫生和计划生育委员会于2015年11月06日《关于发布〈D-二聚体定量检测〉等2项推荐性卫生行业标准的通告》(国卫通〔2015〕15号)发布,自2016年05月01日起实施。
4 发布通知
关于发布《D-二聚体定量检测》等2项推荐性卫生行业标准的通告
国卫通〔2015〕15号
现发布《D-二聚体定量检测》等2项推荐性卫生行业标准,其编号和名称如下:
WS/T 478—2015 血清25-羟基维生素D3检测操作指南
上述标准自2016年 5月1日起施行。
特此通告。
国家卫生计生委
2015年11月6日
5 前言
本标准按照GB/T 1.1—2009给出的规则起草。
本标准起草单位:首都医科大学附属北京世纪坛医院、中国医学科学院北京协和医院、北京医院。
本标准主要起草人:张曼、周慧、邱玲、韩建华、张传宝、张江涛。
6 标准正文
6.1 1 范围
本标准规定了血清25-羟基维生素D3检测的常规方法同位素稀释液相色谱串联质谱法的技术要求,包括试剂配制、样本制备、仪器检测、数据分析等内容。
本标准适用于常规实验室利用同位素稀释液相色谱串联质谱法检测血清25-羟基维生素D3。
6.2 2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
6.3 3 术语和定义
下列术语和定义适用于本文件。
3.1
内标 internal standard
在定量分析时,加入到试样中能与所有组分完全分离的已知量的纯的化合物。
3.2
检出限 limit of detection
由给定测量程序获得的测得值,其声称的物质成分不存在的误判概率为β,声称物质成分存在的误判概率为α。
注1:国际理论和应用化学联合会(IUPAC)推荐α和β的默认值为0.05。
注2:有时使用缩写词LOD。
[JJF 1001—2011,定义7.18]
3.3
线性 linearity
在给定的测量范围内,使测定结果与样本中分析物的量直接成比例的能力。此处的测定结果指最终的分析结果,而非仪器输出的原始信号。
[WS/T 408—2012,定义2.2]
3.4
线性范围 linear range
使实验系统的最终分析结果为可接受的线性的浓度范围,此时非线性误差应低于允许误差。
[WS/T 408—2012,定义2.3]
3.5
基质效应 matrix effect
[WS/T 356—2011,定义2.2]
6.4 4 符号与缩略语
下列符号与缩略语适用于本文件。
25(OH)VD3:25-羟基维生素D3( 25-Hydroxyvitamin D3)
BSA:牛血清白蛋白(bovine serum albumin)
CV:变异系数(coefficient of variation)
LOD:检出限(limit of detection)
MRM:多反应监测(multiple reaction monitor)
SNR:信噪比(signal to noise ratio)
6.5 5 检测原理和方法
本标准建立的25(OH)VD3检测方法以同位素稀释液相色谱串联质谱法为检测原理。方法是以稳定同位素标记的25(OH)VD3为内标添加至血清中,内标与血清均匀混合后,用液液萃取等方法提取血清中25(OH)VD3。加入饱和硫酸锌溶液和乙腈沉淀蛋白,加入正己烷并提取上清液,氮气吹干后,经75%甲醇溶液溶解。利用液相色谱串联质谱分离并检测血清25(OH)VD3和内标特异的离子转变。用25(OH)VD3和内标峰面积比计算血清25(OH)VD3浓度。
6.6 6 试剂和配制
6.6.1 6.1 试剂
可选用的试剂如下:
a) 水:除非有特别说明,应使用GB/T 6682定义的一级实验用水;
b) 甲醇:色谱纯;
e) 甲酸:色谱纯;
f) 硫酸锌七水合物(ZnSO4·7H2O):分析纯,CAS号:7446-20-0;
g) 四氘代甲醇(d4-甲醇):纯度≥99.9%,CAS号:811-98-3;
h) 磷酸氢二钠七水合物( Na2HPO4·7H2O):分析纯,CAS号:7782-85-6;
i) 磷酸二氢钠一水合物(Na2HPO4·H2O):分析纯,CAS号:10049-21-5;
k) 牛血清白蛋白(BSA):纯度≥98%,Mr=66 kDa,CAS号:9048-46-8;
6.6.2 6.2 配制溶液
6.6.2.1 6.2.1 空白基质溶液
模拟人血清基质的条件,选择适当离子强度、适当pH及蛋白成分的物质进行配制,尽量模拟人血清基质的环境。如获得人血清纯化后无25(OH)VD3的空白基质,则更佳。适用时,可采用下述方法进行:
a) 称量2.140 g磷酸氢二钠七水化合物(Na2HPO4·7H2O),0.268 g磷酸二氢钠一水化合物(NaH2PO4·H20),0.900 g氯化钠,5.000 g牛血清白蛋白;
b) 溶解于约75 mL水中;
d) 转移到100 mL容量瓶中;
e) 加水定容至规定刻度。
6.6.2.2 6.2.2 饱和硫酸锌溶液
适用时,可采用下述方法进行配制:
a) 称量9.50 g硫酸锌七水化合物(ZnSO4·7H2O);
b)加入10 mL水;
c) 充分混匀5 min;d)静置1 min;
e) 再次混匀2 min以上,至无大块颗粒不溶物为止。
最终配制的溶液中硫酸锌七水化合物(ZnSO4·7H2O)浓度为0.2 mol/L。该溶液2℃~8℃稳定性为1个月。
6.6.2.3 6.2.3 75%甲醇溶液
适用时,可采用下述方法进行配制:
a) 移取30 mL甲醇;
b) 加入10 mL水;
c) 混匀后,加入40 μL甲酸;
d)充分混匀。
6.6.2.4 6.2.4 流动相A
适用时,可采用甲酸水溶液,含0.1%甲酸的水溶液的配制方法为移取300 mL水,加入300μL甲酸。流动相宜每日新鲜配制,可根据使用量适当调整。
6.6.2.5 6.2.5 流动相B
适用时,可采用甲酸甲醇溶液。含0.1%甲酸的甲醇溶液的配制方法为移取300 mL甲醇,加入300μL甲酸。甲醇为易挥发溶剂,宜根据每日使用量进行配制。
6.7 7 仪器
6.7.1 7.1 液相色谱串联质谱联用系统
液相色谱串联质谱联用系统应满足以下使用要求:
a) 高效液相色谱仪;
b) 三重四级杆串联质谱仪,配有稳定的源,如电喷雾离子源(ESI),质量校正合格,各项参数指标符合正常工作的要求。
6.7.2 7.2 液相色谱柱
液相色谱柱应满足使用以下要求:
a) 反相C18色谱柱,具有良好稳定性和重现性;b) 规格内径和理论塔板数满足使用要求。
6.7.3 7.3 天平
万分之一天平(最小分度0.1 mg),应校准合格并在强制检定周期内。
十万分之一天平(最小分度0.01 mg),应校准合格并在强制检定周期内。
6.7.4 7.4 容量瓶
精度为标称容量±O.10 mL。
6.7.5 7.5 离心机
6.7.6 7.6 旋涡式混合器
6.7.7 7.7 吹干装置
可连接氮气源的吹干装置。
6.7.8 7.8 微量移液器
经校准合格的微量移液器,规格1000 μL、200μL和20μL移液器各一支。
6.7.9 7.9 离心管
适用时,可选用规格1.5 mL,离心管材质中无可经有机溶剂萃取出的杂质。
6.8 8 样本
6.8.1 8.1 通则
本方法适用于新鲜、冰冻或冻干血清样本的25(OH)VD3浓度检测。
在处理样本时,应严格遵从对潜在生物传染性样本处理的相关规定,使用时遵循生物安全规则,并根据规定对废物进行处理。
6.8.2 8.2 样本用量
最小取样量不宜低于0.15 mL。
6.8.3 8.3 样本的保存
新鲜血清样本若不立即检测,应于2℃~8℃避光保存,保存时间不超过1周。-20℃及以下避光可稳定保存至少3个月。使用前应在室温下避光将血清融化、充分混匀。冻干样本应按照介绍描述的使用期限和条件保存,临用前按照说明复融重组,充分混匀。
6.9 9 检测系统和分析部分的准备
6.9.1 9.1 液相色谱串联质谱联用系统的准备
6.9.1.1 9.1.1 质谱系统部分的准备
c) 真空度达到正常工作要求的范围,所需辅助气体纯度符合要求、供应充足、气路通畅。
6.9.1.2 9.1.2 液相系统部分准备
a) 流动相准备:按照6.2.4,6.2.5准备流动相A,流动相B,超声10 min~15 min;
b)色谱柱的平衡:用合适的流动相比例(例如A:B体积比20:80)平衡色谱柱一定时间,直至色谱柱压力达到平衡。
6.9.2 9.2 标准溶液和内标溶液的准备
6.9.2.1 9.2.1 标准品
6.9.2.1.1 9.2.1.125(OH)VD3标准品
纯度≥99%。
6.9.2.1.2 9.2.1.2 同位素标记物质
应使用稳定同位素标记的25(OH)VD3为内标,标记的稳定同位素个数应不低于3个。内标的使用、保存及使用期限应符合生产厂商提供的产品证书或使用说明书。
6.9.2.2 9.2.2 标准溶液及内标溶液的制备
a) 称取25(OH)VD3标准品1.00 mg;
c) 充分混匀。
9.2.2.2 1 mg/mL内标储备液
配制方法如下:
a) 称取同位素标记的25(OH)VD31.00 mg;
c) 充分混匀1 min。
9.2.2.3 内标工作液配制方法如下:
a) 取0.010 mL已制备的1 mg/mL内标储备液,加入0.990 mL甲醇,配成浓度为10 μg/mL的基础工作液;
b)取0.100 mL已制备的10 μg/mL基础工作液,加入0.900 mL甲醇,配成浓度为1μg/mL的内标工作液。
a) 取0.010 mL已制备的2 mg/mL标准品储备液,加入0.990 mL甲醇,充分混匀,得到浓度为20 μg/mL的标准品基础工作液1;
b)取0.100 mL标准品基础工作液1,加入0.900 mL甲醇,充分混匀,得到浓度为2μg/mL的标准品基础工作液2;
c) 将标准品基础工作液2按照1:2:2:2:2:1.25:2:5配制标准品基础工作液3~9,溶剂为甲醇。分别得到浓度为1 μg/mL,0.5 μg/mL,0.25μg/mL,0.125μg/mL,O.1μg/mL,0.05μg/mL,0.01 μg/mL的标准品基础工作液。
a) 分别取不同浓度的标准品基础T作液2~9各0.100 mL;
c) 充分混匀,得到浓度分别为0.2 μg/mL,0.1μg/mL,0.05 μg/mL,0.025 μg/mL,0.0125μg/mL,0.01μg/mL,0.005μg/mL,0.001μg/mL的标准品T作液。
9.3 样本前处理(包括标准品工作液和待测血清样本)样本前处理方法如下:
a) 移取血清样本或标准品T作液0.150 mL,加入0.015 mL内标T作液(浓度为1μg/mL),充分混匀;
c) 加入乙腈0.300 mL;
d) 剧烈震荡30 s,室温(22℃~28℃)静置15 min;
e) 加入正己烷0.750 mL;
f) 剧烈震荡30 s;
h) 可见样本分为三层,取最上层有机层0.500 mL于另一离心管中,注意不要触及中间的水层;
i) 室温下氮气吹干;
j) 加入75%甲醇溶液0.200 mL;k)充分混匀30 s。
6.9.3 9.4 检测方法
6.9.3.1 9.4.1 液相色谱条件
6.9.3.1.1 9.4.1.1 液相色谱仪器条件
使用者可以实现目标物与基质干扰物的充分分离,以及实现目标物与其他分析物有效分离并获得良好峰型为原则进行条件优化,包括:
a) 色谱柱:见7.2;
b) 流动相:见9.1.2;
c) 流速:0.5 mL/min;
d) 进样量:0.010 mL;
e) 柱温:50℃。
6.9.3.1.2 9.4.1.2 液相色谱洗脱条件
使用者可根据实验需要进行条件优化,见表1。
表1 液相色谱洗脱条件
时间 min | 流动相A % | 流动相B / |
0 | 20 | 80 |
2.3 | 20 | 80 |
2.4 | 2 | 98 |
3.9 | 2 | 98 |
4 | 20 | 80 |
6.9.3.2 9.4.2 质谱条件
使用者可以有效提高离子化效率为原则,优化离子源的类型、温度,以及雾化器、干燥器温度和流量等参数;以有效提高离子传输效率为原则,优化锥孔电压,碰撞能量等参数,进而实现提高检测灵敏度的目的,合理选择反应模式,进行条件优化,见表2。
表2 串联质谱检测条件
源 | 反应模式 | 雾化器压力 kPa(psi) | 干燥器 | 母离子 m/z | 子离子 m /z | 锥孔电压 V | 碰撞能量 eV | 驻留时间 | ||
ESI | 345(50) | 温度 ℃ | 流速 L/min | 25(OH)VD3 | 401.3 | 383.2a | 106 | 4 | 0.1 | |
159.1 | 106 | 24 | 0.1 | |||||||
275 | 10 | 同位素标记25(OH)VD3 | 404.4 | 386.3 | 106 | 4 | 0.1 | |||
a离子用于定量。 | ||||||||||
6.9.3.3 9.4.3 液相色谱串联质谱检测
按照以下步骤进行液相色谱串联质谱检测:
a) 按照9.3方法对标准品T作液和待测血清样本进行前处理,按照9.4.1~9.4.2条件进行液相色谱串联质谱参数设置和优化;
b) 标准品工作液经前处理后,按照浓度由低到高顺序进行液相色谱串联质谱分析;
6.9.3.4 9.4.4 结果计算
6.9.3.4.1 9.4.4.1 保留时间
25(OH)VD3在液相色谱中保留时间可依使用的色谱柱性能不同而有差异,建议与标准品溶液保留时间差值小于0.1 min。
6.9.3.4.2 9.4.4.2 工作曲线的建立
9.4.4.2.1 直线拟合
对25(OH)VD3和同位素标记25(OH) VD3按表2分别提取MRM离子色谱图,积分得各自的峰面积。以标准品定量离子峰面积与内标峰面积的比值为纵坐标,以标准品浓度与内标物浓度的比值为横坐标进行直线拟合,按式(1)得到工作曲线参数a,b值。
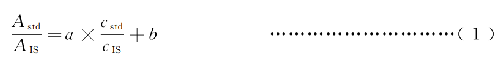
![]()
式中:
Astd——标准品T作液中25(OH)VD3定量离子MRM积分峰面积;
cstd——标准品工作液中25(OH)VD3的浓度;
cIS——标准品工作液中内标物的浓度,本方案中此浓度为1μg/mL;
α——拟合直线的斜率;
b——拟合直线的截距。
直线拟合的相关系数R2>0.99。
9.4.4.2.2 建立工作曲线
将9.4.4.2.1中拟合得到的参数a,b带人式(2),得到工作曲线。

式中: Atarget——血清样本中25(OH)VD3定量离子MRM积分峰面积;
cIS——血清样本中内标物的浓度,本方案中此浓度为1 μg/mL;
a——按照9.4.4.2.1中拟合得到的直线斜率;
b——按照9.4.4.2.1拟合得到的直线截距。
对血清样本中25(OH)VD3和同位素标记25(OH)VD3按照表2分别提取MRM离子色谱图,积分得各白的峰面积。根据9.4.4.2.2得到的T作曲线,可计算得到式(2)中ctarget值,即血清样本中25(OH)VD3的浓度。
6.10 10 方法的评价
6.10.1 10.1 说明
实验条件优化后,需对方法进行多方面评价,例如精密度,正确度,线性,LOD,基质效应等。
6.10.2 10.2 精密度评价
依据临床实验室标准化委员会( Clinical and Laboratory Standards Institute,CLSI)公布或者已发布的行业标准等规范性文件,对方法的精密度进行评价,见表3。
表3 精密度评价结果
6.10.3 10.3 正确度评价
适用时,可利用有证标准物质或者其他规范性文件方案进行评价,正确度评价结果在靶值±5%范围内。
6.10.4 10.4 线性评价
依据CLSI公布或者已发布的行业标准等规范性文件,对方法的线性进行评价:
检测血清样本的线性范围10.16 ng/mL~70.54 ng/mL。如收集到足量的更低浓度血清样本,经验证后,可扩大线性范围的低限;如获得加入纯物质的更高值人血清,经验证后,可扩大线性范围的高限。
注:受标本本身浓度限制,高值血清为人血清加入纯物质获得,低值血清为收集人血清。
6.10.5 10.5 LOD
按照SNR≥3的最低浓度计算,例如检出限为0.5 ng/mL。
6.10.6 10.6 基质效应
依据行业内或专业领域认可的规范性文件,评价不同浓度时的基质效应:
7 参考文献
[1] Susan S.-C.Tai, Mary Bedner, Karen W. Phinney. Development of a Candidate ReferenceMeasurement Procedure for the Determination of 25-Hydroxyvitamin D3 and 25-Hydroxyvitamin D2 inHuman Serum Using Isotope-Dilution Liquid Chromatography-Tandem Mass Spectrometry. Anal.Chem.2010,82,1942-1948.
[2] Stepman HC, Vanderroost A, van Uytfanghe K, et al. Candidate reference measurementprocedures for serum 25-hydroxyvitamin D3 and 25-hydroxyvitamin D2 by using isotope-dilution liquidchromatography-tandem mass spectrometry[J].Clin Chem,2011,57(3):441-448.